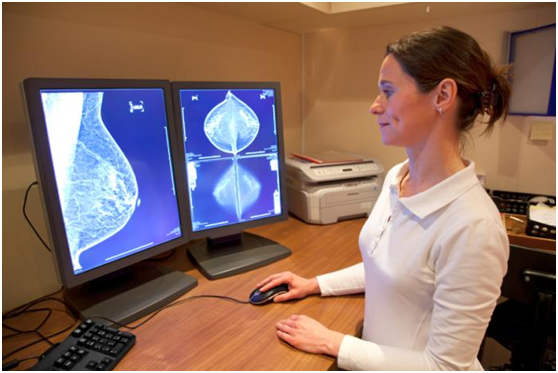
2022年8月29日,由中国医学科学院肿瘤医院王燕教授团队开展的吡咯替尼联合Apatinib/ target=_blank class=infotextkey>阿帕替尼用于HER2突变非小细胞肺癌(NSCLC)的前瞻性、开放标签、单臂Ⅱ期临床研究结果在线发表于BMC Medicine(IF:11.150)[1],研究结果显示吡咯替尼联合Apatinib/ target=_blank class=infotextkey>阿帕替尼的客观缓解率(ORR)为51.5%,疾病控制率(DCR)为93.9%,中位无进展生存期(PFS)为6.9个月,总生存期(OS)为14.8个月,安全性良好。
吡咯替尼联合阿帕替尼用于HER2突变晚期非小细胞肺癌发表于BMC Medicine
NSCLC是一种基因多样性异质性恶性肿瘤,HER2突变约占NSCLC患者的2%~4%,主要表现为蛋白过表达、基因扩增或基因突变[2,3]。HER2突变NSCLC常见于女性、不吸烟肺腺癌患者。与无HER2突变或其他分子突变的患者相比,此类患者发生脑转移的概率更高[2,4,5]。
HER2突变患者对酪氨酸激酶抑制剂(TKIs)相对不敏感,ORR低于30%[6-9]。HER2突变人群的标准治疗仍是化疗或免疫治疗,临床获益也有限[10-12]。目前只有两种抗HER2抗体药物偶联物(ADCs),曲妥珠单抗-美坦新偶联物(ado-T-DM1)和德喜曲妥珠单抗(T-DXd)/ target=_blank class=infotextkey>DS-8201)在HER2突变NSCLC中显示出令人鼓舞的疗效,ORR为44%~55%[13,14]。然而,肺毒性可能会限制它们的应用。因此,需要探索更多的抗HER2治疗方法。
肿瘤血管生成是肿瘤发病机制的重要特征,不仅为肿瘤提供氧气,而且为癌细胞的转移扩散提供了重要途径[15]。抗血管生成药物靶向血管内皮生长因子(VEGF)和VEGF受体(VEGFR),使病理性肿瘤血管正常化,调节肿瘤微环境,抑制新生血管生成[15,16]。已有研究表明,EGFR-TKIs与抗血管生成药物联合使用时,可使晚期NSCLC患者生存显著获益[17-19]。VEGF的表达也受到HER2信号的调控,且抑制VEGF/VEGFR活性会增强HER2抑制剂的抗肿瘤作用[20]。
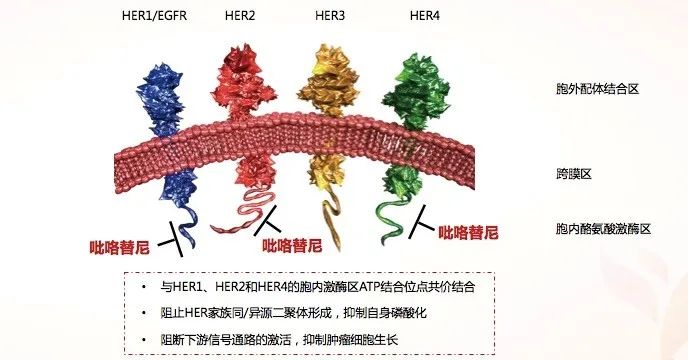
吡咯替尼是一种不可逆的口服泛ErbB TKI,靶向EGFR/HER1、HER2和HER4。一项Ⅱ期研究显示,吡咯替尼单药治疗二线或二线以上HER2突变NSCLC患者,ORR为30%,安全性良好[21]。阿帕替尼是选择性靶向VEGFR-2的口服小分子TKI,阿帕替尼联合化疗或EGFR-TKI治疗晚期NSCLC显示临床获益[18,22]。此外,体外研究显示阿帕替尼联合吡咯替尼具有协同抗肿瘤作用[23]。
本研究是一项单臂Ⅱ期临床研究,探讨吡咯替尼联合阿帕替尼用于HER2突变或扩增晚期NSCLC患者的疗效和安全性。研究入组一线化疗或EGFR TKI治疗失败HER2突变或HER2扩增的晚期NSCLC患者,口服吡咯替尼400mg qd+阿帕替尼250mg qd,直至疾病进展、不可耐受的毒性或死亡。主要终点为研究者判定的客观缓解率。
2019年3月至2020年12月,本研究共纳入33例肺腺癌患者,中位年龄54(范围,35~70)岁。在33例患者中,28例(84.8%)是HER2 20外显子插入突变,3例患者携带HER2 TKD错义突变,其余2例为原发性HER2扩增。截至2021年9月20日,中位持续治疗时间为6.9个月,3例患者(9.1%)仍在接受治疗,中位随访时间为11.3个月。
在33例可评估的患者中,17例(51.5%)PR,14例(42.4%)SD,研究者评估的ORR为51.5%,DCR为93.9%。84.8%(28/33)的患者靶病灶大小较基线减小(图1)。

图1. 最佳缓解瀑布图
中位缓解持续时间(DOR)为6.0个月,中位PFS为6.9个月(图2A和2B)。在数据截止时,33例患者中有18例(54.5%)死亡,中位OS为14.8个月(图2C),1年总生存率为58.9%。



图2. 缓解持续时间(A)、无进展生存期(B)和总生存期(C)Kaplan-Meier分析
事后亚组分析,吡咯替尼联合阿帕替尼二线治疗与三线及三线以上治疗ORR相似,分别为52.9%和50.0%。二线治疗和后线治疗的中位PFS时间分别为8.5个月和6.2个月。基线无脑转移和有脑转移,ORR分别为50.0%和53.8%,中位PFS时间分别为7.0个月和6.7个月。HER2 20外显子插入的患者,YVMA插入患者和YVMA未插入患者的中位PFS时间分别为5.9个月和7.7个月(图3)。
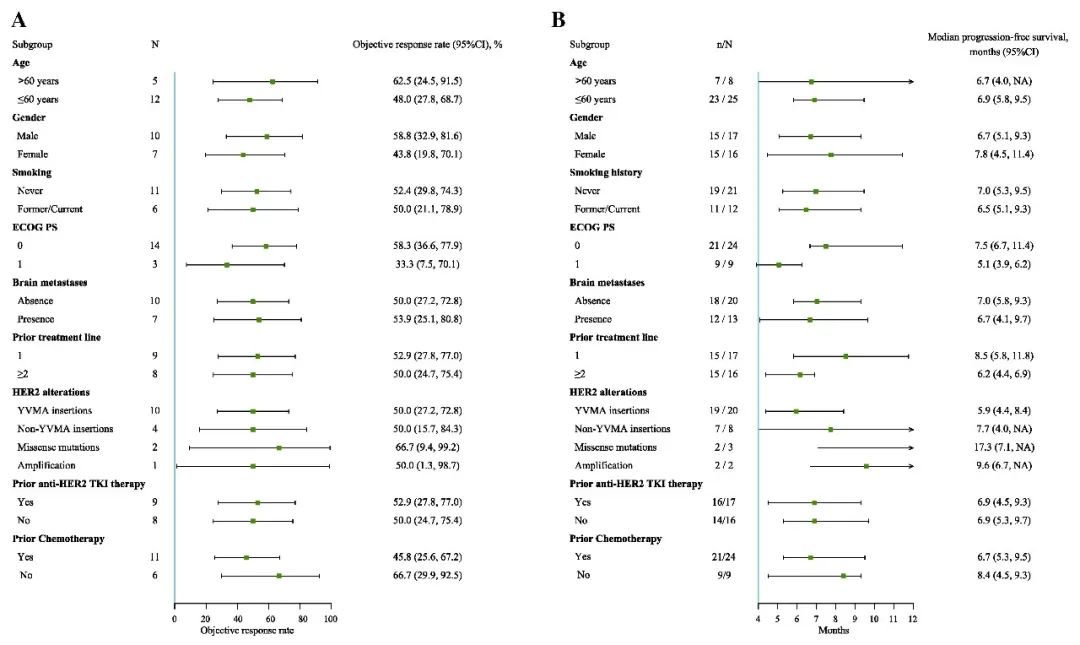
图3. 客观缓解率(A)和无进展生存期(B)亚组分析
绝大多数TRAE为1级或2级,最常见的是腹泻(90.9%)、高血压(72.7%)、厌食(54.5%)、恶心(51.5%)和口腔粘膜炎(45.5%)。3级TRAE主要为腹泻(3.0%)和高血压(9.1%)。未见4级或5级TRAE报告。
本研究是首个探索HER2靶向TKI药物联合抗血管生成药物治疗至少一线治疗失败的HER2突变晚期NSCLC患者疗效和安全性的试验,试验达到了主要终点,ORR为51.5%。此外,DCR为93.9%,中位DoR为6.0个月,中位PFS为6.9个月,中位OS为14.8个月。研究显示出令人鼓舞的抗肿瘤活性和良好的安全性,提示吡咯替尼联合阿帕替尼是治疗HER2突变或扩增NSCLC的有效策略。
同时亚组分析表明,吡咯替尼联合阿帕替尼治疗二线或三线及以上的NSCLC患者,疾病缓解相似,但二线治疗患者的PFS优于三线或三线以上治疗患者(9.8个月vs.6.1个月),表明对于HER2突变的NSCLC患者,更早线使用吡咯替尼联合阿帕替尼可能更有效,然而这需要开展进一步的研究来证实。
参考文献
1. Yang G, Xu H, Yang Y, et al. Pyrotinib combined with apatinib for targeting metastatic non-small cell lung cancer with HER2 alterations: a prospective, open-label, single-arm phase 2 study (PATHER2). BMC Med. 2022 Aug 29;20(1):277. doi: 10.1186/s12916-022-02470-6.
2. Arcila ME, Chaft JE, Nafa K, Roy-Chowdhuri S, Lau C, Zaidinski M, et al. Prevalence, clinicopathologic associations, and molecular spectrum of ERBB2 (HER2) tyrosine kinase mutations in lung adenocarcinomas. Clin Cancer Res. 2012;18(18):4910-8.
3. Mazières J, Peters S, Lepage B, Cortot AB, Barlesi F, Beau-Faller M, et al. Lung cancer that harbors an HER2 mutation: epidemiologic characteristics and therapeutic perspectives. J Clin Oncol. 2013;31(16):1997-2003.
4. Bu S, Wang R, Pan Y, Yu S, Shen X, Li Y, et al. Clinicopathologic characteristics of patients with HER2 insertions in non-small cell lung cancer. Ann Surg Oncol. 2017;24(1):291-7.
5. Offin M, Feldman D, Ni A, Myers ML, Lai WV, Pentsova E, et al. Frequency and outcomes of brain metastases in patients with HER2-mutant lung cancers. Cancer. 2019;125(24):4380-7.
6. Dziadziuszko R, Smit EF, Dafni U, Wolf J, Was?g B, Biernat W, et al. Afatinib in NSCLC with HER2 mutations: results of the prospective, open-label phase Ⅱ NICHE trial of European Thoracic Oncology Platform (ETOP). J Thorac Oncol. 2019;14(6):1086-94.
7. Elamin YY, Robichaux JP, Carter BW, Altan M, Gibbons DL, Fossella FV, et al. Poziotinib for patients with HER2 exon 20 mutant non-small-cell lung cancer: results from a phase Ⅱ trial. J Clin Oncol. 2022;40(7):702-9.
8. Hyman DM, Piha-Paul SA, Won H, Rodon J, Saura C, Shapiro GI, et al. HER kinase inhibition in patients with HER2- and HER3-mutant cancers. Nature. 2018;554(7691):189-94.
9. Kris MG, Camidge DR, Giaccone G, Hida T, Li BT, O'Connell J, et al. Targeting HER2 aberrations as actionable drivers in lung cancers: phase Ⅱ trial of the pan-HER tyrosine kinase inhibitor Dacomitinib in patients with HER2-mutant or amplified tumors. Ann Oncol. 2015;26(7):1421-7.
10. Hanna NH, Robinson AG, Temin S, Baker S, Jr., Brahmer JR, Ellis PM, et al. Therapy for stage IV non-small-cell lung cancer with driver alterations: ASCO and OH (CCO) joint guideline update. J Clin Oncol. 2021;39(9):1040-91.
11. Mazieres J, Drilon A, Lusque A, Mhanna L, Cortot AB, Mezquita L, et al. Immune checkpoint inhibitors for patients with advanced lung cancer and oncogenic driver alterations: results from the IMMUNOTARGET registry. Ann Oncol. 2019;30(8):1321-8.
12. Zhou J, Ding N, Xu X, Zhang Y, Ye M, Li C, et al. Clinical outcomes of patients with HER2-mutant advanced lung cancer: chemotherapies versus HER2-directed therapies. Ther Adv Med Oncol. 2020;12:1758835920936090.
13. Li BT, Shen R, Buonocore D, Olah ZT, Ni A, Ginsberg MS, et al. Ado-tRAStuzumab emtansine for patients with HER2-mutant lung cancers: results from a phase Ⅱ basket trial. J Clin Oncol. 2018;36(24):2532-7.
14. Li BT, Smit EF, Goto Y, Nakagawa K, Udagawa H, Mazières J, et al. TRAStuzumab deruxtecan in HER2-mutant non-small-cell lung cancer. N Engl J Med. 2022;386(3):241-51.
15. Jain RK. Normalization of tumor vasculature: an emerging concept in antiangiogenic therapy. Science. 2005;307(5706):58-62.
16. Folkman J. Tumor angiogenesis: therapeutic implications. N Engl J Med. 1971;285(21):1182-6.
17. Saito H, Fukuhara T, Furuya N, Watanabe K, Sugawara S, Iwasawa S, et al. Erlotinib plus Bevacizumab versus erlotinib alone in patients with EGFR-positive advanced non-squamous non-small-cell lung cancer (NEJ026): interim analysis of an open-label, randomised, multicentre, phase 3 trial. Lancet Oncol. 2019;20(5):625-35.
18. Zhao H, Yao W, Min X, Gu K, Yu G, Zhang Z, et al. Apatinib plus Gefitinib as first-line treatment in advanced EGFR-mutant NSCLC: the phase Ⅲ ACTIVE study (CTONG1706). J Thorac Oncol. 2021;16(9):1533-46.
19. Larsen AK, OuaRET D, El Ouadrani K, Petitprez A. Targeting EGFR and VEGF(R) pathway cross-tALK in tumor survival and angiogenesis. Pharmacol Ther. 2011;131(1):80-90.
20. Kerbel R, Folkman J. Clinical translation of angiogenesis inhibitors. Nat Rev Cancer. 2002;2(10):727-39.
21. Zhou C, Li X, Wang Q, Gao G, Zhang Y, Chen J, et al. Pyrotinib in HER2-mutant advanced lung adenocarcinoma after platinum-based chemotherapy: a multicenter, open-label, single-arm, phase Ⅱ study. J Clin Oncol. 2020;38(24):2753-61.
22. Zhang X, Xiong Y, Xia Q, Wu F, Liu L, Zhou Y, et al. Efficacy and safety of apatinib plus vinorelbine in patients with wild-type advanced non-small cell lung cancer after second-line treatment failure: a nonrandomized clinical Trial. JAMA Netw Open. 2020;3(3):e201226.
23. Su B, Huang T, Jin Y, Yin H, Qiu H, Yuan X. Apatinib exhibits synergistic effect with pyrotinib and reverses acquired pyrotinib resistance in HER2-positive gastric cancer via stem cell factor/c-Kit signaling and its downstream pathways. Gastric Cancer. 2021;24(2):352-67.